- Γράφει ο Κοσμάς Ζακυνθινός
Το «πράσινο φως» έδωσε η Επιτροπή Φαρμάκων για Ανθρώπινη Χρήση (CHMP) για την κυκλοφορία του νέου σκευάσματος Wegovy της Novo Nordisk, το οποίο προορίζεται για τη θεραπεία ατόμων με παχυσαρκία.
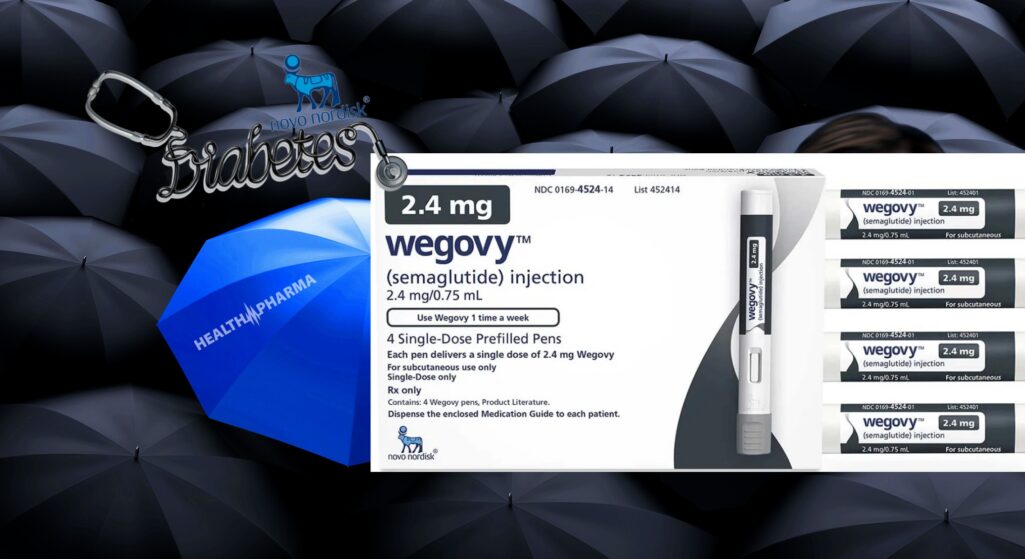
Το Wegovy θα είναι διαθέσιμο ως ενέσιμα διαλύματα των 0,25 mg, 0,5 mg, 1 mg, 1,7 mg και 2,4 mg. Η δραστική ουσία του Wegovy είναι η σεμαγλουτίδη, ένας αγωνιστής (ATC: A10BJ06) του υποδοχέα του παρόμοιου με τη γλυκαγόνη πεπτιδίου-1 (GLP-1). Ο μηχανισμός με τον οποίο η θεραπεία με σεμαγλουτίδη οδηγεί σε απώλεια βάρους δεν είναι πλήρως κατανοητός. Ωστόσο, μεταξύ των άλλων λειτουργιών, το GLP-1. φαίνεται να ρυθμίζει την όρεξη, αυξάνοντας τα αισθήματα κορεσμού και πληρότητας. Ταυτόχρονα, μειώνει τα αισθήματα πείνας και περιορίζει τη διάθεση για πρόσληψη ενέργειας.
Το όφελος του Wegovy αποδείχθηκε σε κλινική μελέτη, αποδεικνύοντας τη σχετική επίδραση του στην απώλεια βάρους, όταν χρησιμοποιείται σε συνδυασμό με δίαιτα μειωμένων θερμίδων και αυξημένη σωματική δραστηριότητα για τη διαχείριση του βάρους σε άτομα με παχυσαρκία.
Σύμφωνα με την ανακοίνωση που εξέδωσε η CHMP για το Wegovy, η πλήρης ένδειξη είναι του φαρμάκου είναι:
Το Wegovy ενδείκνυται συμπληρωματικά μαζί με δίαιτα μειωμένων θερμίδων και αυξημένη σωματική δραστηριότητα για τη διαχείριση βάρους, συμπεριλαμβανομένης της απώλειας βάρους και της διατήρησης του, σε ενήλικες με αρχικό Δείκτη Μάζας Σώματος (ΔΜΣ):
- ≥30 kg/m2 (παχυσαρκία) ή
- ≥27 kg/m2 έως <30 kg/m2 (υπέρβαρος) παρουσία τουλάχιστον μιας συννοσηρότητας που σχετίζεται με τα επιπλέον κιλά, όπως π.χ. δυσγλυκαιμία (προδιαβήτης ή σακχαρώδης διαβήτης τύπου 2), υπέρταση, δυσλιπιδαιμία, αποφρακτική άπνοια ύπνου ή καρδιαγγειακή νόσο.
Λεπτομερείς συστάσεις για τη χρήση αυτού του προϊόντος θα περιγράφουνε στην περίληψη. των χαρακτηριστικών του προϊόντος (SmPC), η οποία θα δημοσιευθεί στην Ευρωπαϊκή. έκθεση αξιολόγησης (EPAR) και θα είναι διαθέσιμη σε όλες τις επίσημες γλώσσες της. Ευρωπαϊκής Ένωσης μετά τη χορήγηση της άδειας κυκλοφορίας από την Ευρωπαϊκή. Επιτροπή.
Εντυπωσιακή μείωση βάρους
Στις μελέτες που παρουσιάστηκαν από την Novo Nordisk για την έγκριση από την. Αμερικανική Υπηρεσία Τροφίμων και Φαρμάκων (FDA), δεν υπήρξαν διατροφικές. παρεμβάσεις και πρόγραμμα άσκησης, σε αυτές συμπεριλήφθηκαν και τα άτομα με Διαβήτη. (STEP 1, 2, 4), παρατηρήθηκε εντυπωσιακή μείωση του σωματικού βάρους. Συγκεκριμένα. σημειώθηκε ποσοστό μείωσης του σωματικού βάρους κατά 15-18%, σε όλη την διάρκεια. των 68 εβδομάδων.
Συνολικά, το 70% των συμμετεχόντων έχασαν τουλάχιστον το 10% του βάρους τους, ενώ ένα 20% απώλεσε το 20% των κιλών του. Τα ποσοστά αυτά είναι διπλάσια από κάθε άλλο. φάρμακο που κυκλοφορεί για την παχυσαρκία.
Οι παρενέργειες που αναφέρθηκαν αφορούσαν μόνο γαστρεντερικές ενοχλήσεις, οι οποίες όμως ήταν παροδικές. Μελέτες καρδιαγγειακής ασφάλειας βρίσκονται σε εξέλιξη με το. πρόγραμμα Semaglutide Effects on Heart Disease and Stroke in Patients With Overweight. or Obesity (SELECT) trial, το οποίο θα είναι έτοιμο το 2023.
Κάντε like στη σελίδα μας στο facebook για να μαθαίνετε όλα τα νέα